百万元的抗癌药,有望大幅降价? 商保或成新出路
抗癌药有望纳入商业保险,特别是那些价格高昂的药物。10月底,国家医疗保障局开展了2025年国家基本医保药品目录谈判和商保创新药目录价格协商工作,商保创新药目录首次引入谈判。天津合源生物科技有限公司谈判代表结束价格协商后对结果持明显乐观态度。该企业的纳基奥仑赛是国内首款治疗白血病的CAR-T产品,定价为每针99.9万元,已是国内CAR-T类产品的最低价。
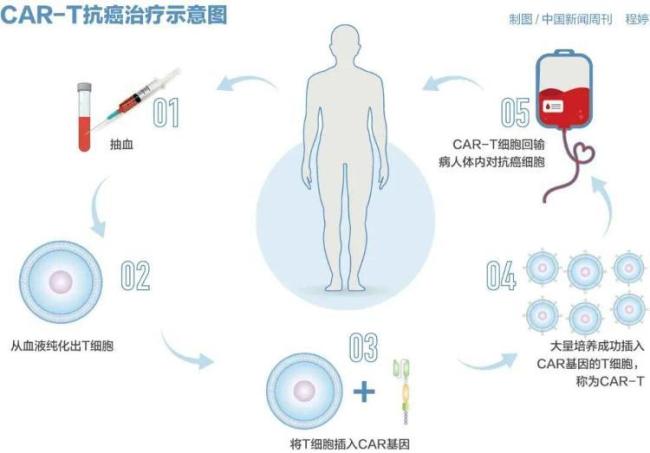
CAR-T疗法即嵌合抗原受体T细胞免疫疗法,从患者或供体采集的免疫细胞经基因改造,装备上能识别癌细胞的“精准导航系统”(CAR),回输至患者体内后,这支升级版的免疫军队能精准高效地歼灭癌细胞。目前国内共有8款CAR-T产品获国家药监局批准上市,一针定价大多高达百万元。

中国科学技术大学附属第一医院风湿免疫科主任陈竹表示,CAR-T疗法正在向低成本、低风险方向迈进。他和团队近期开展了针对系统性红斑狼疮的CAR-T疗法临床研究,并取得关键进展,成果今年9月刊发于国际期刊《新英格兰医学杂志》。
然而,从百万元到平价,CAR-T疗法需要的不只是技术革新。今年9月,国务院发布《生物医学新技术临床研究和临床转化应用管理条例》,自明年5月1日起施行。该条例旨在规范生物医学新技术临床研究和转化应用,被称为细胞治疗等前沿疗法的“基本法”。
自身免疫性疾病常被形容为身体里的一场“兵变”。以系统性红斑狼疮(SLE)为例,患者最具特征性的临床表现便是面部的蝶形红斑。原本应攻击外来入侵者的免疫系统,把自身血管当成敌人攻击,从而出现体表溃烂、瘢痕等。据北京协和医院风湿免疫科团队2024年发表于国内期刊《科学通报》上的流行病学调查,SLE常见于育龄期女性,且国内发病率正逐年上升。
SLE的传统疗法都是对症治疗,通过抑制免疫系统功能来缓解症状,常用治疗药物是糖皮质激素和免疫抑制剂。由于无法根治,患者停药之后病情会复发。若长期用药,对部分患者而言,药效会减退。此外,激素和免疫抑制剂通常伴有不良反应,并非长久之计。
CAR-T疗法的出现改变了这一状况。2012年,一位叫艾米丽的患急性淋巴性白血病的女孩,在美国接受了这一疗法,健康存活至今。2017年,美国食品药品监督管理局(FDA)率先批准了针对血液系统恶性肿瘤的CAR-T疗法。国内同类药物的首次获批则是在2021年。
寻找精准定位“敌人”的方法是CAR-T疗法的关键。多项临床研究证实,其能有效清除组织脏器中的B细胞。B细胞清除得越彻底,疾病获得长期缓解的概率就越大。传统的CAR-T疗法需要把人体血液中的T细胞抽取出来进行培养。这些取出的T细胞经过一系列体外处理,通过基因编辑等手段令其产生与抗癌相关的抗原,再经过培养、扩增和检测后回输给患者。这些装备了“肿瘤定位导航”的超级T细胞能在患者体内精准识别并杀伤癌细胞。
但这一流程存在显而易见的问题。回输前患者要做一系列准备,比如要停用免疫抑制剂,减小激素剂量,并等待体外T细胞的培养。整个过程可能持续两周到一个月。这也意味着,部分重病患者等不起。此外,绝大多数研究方案中,患者治疗前要接受预处理,包括用药物清扫淋巴,相当于削弱了人体的免疫防线,会增加感染风险。
异体通用型CAR-T是一种思路。去年7月,上海邦耀生物科技有限公司与上海长征医院合作,研发出新一代异体通用型CAR-T疗法,3名患有复发难治性自身免疫性疾病的患者接受该疗法后,病情得到明显改善。该成果发表于《细胞》,并入选当年《细胞》年度最佳论文。
华东师范大学生命医学研究所所长、邦耀生物创始人刘明耀指出,目前国内外已获批的CAR-T疗法都是自体CAR-T,也就是取患者自己的T细胞进行改造培养。但肿瘤患者此前大多经过放化疗,其T细胞有着诸多缺陷。异体CAR-T从年轻健康的供体获取T细胞,其功能显然更强。但异体CAR-T要解决两个重大问题:异体的T细胞会攻击患者的健康组织器官,引发强烈免疫反应;其次,便是患者对异体细胞的免疫排异。
邦耀生物从2016年便开始解决异体T细胞的排异问题。刘明耀回忆,团队通过基因编辑手段敲除或加入某些基因,让异体T细胞能在患者体内正常扩增。2018年,第一批通用CAR-T细胞就做出来了,但一上临床就发现,受试患者的免疫排异非常显著。经过八年多的迭代,刘明耀团队终于证明了异体CAR-T在患者体内能免于排异,且无强烈免疫反应发生。
在刘明耀看来,异体CAR-T的一大优势在于一份T细胞可以在体外扩增,制备成百上千份的“救命药”。和普通细胞药物一样,异体CAR-T可以做好放在冰箱里储存起来,随时取用。
另一种思路是把T细胞的体外改造过程搬到患者体内。这便是陈竹团队的最新成果。传统T细胞的体外改造通常选用病毒载体对细胞DNA进行编辑,为其装配精准导航。而直接在体内生成 CAR-T 细胞只需要几小时。
国际上,体内CAR-T疗法已成为投融资合作的新焦点。今年3月,药企巨头阿斯利康以10亿美元收购了比利时EsoBiotec公司,以获得其体内CAR-T技术平台。8月,美国吉利德科学公司旗下的老牌CAR-T巨头Kite以3.5亿美元收购了一家专注体内CAR-T疗法的私营生物技术公司。CAR-T疗法正完成一场技术蝶变。
全球范围内尚未有CAR-T疗法正式获批用于治疗自身免疫性疾病。邦耀生物在研的异体CAR-T疗法有两个适应证:一是血液肿瘤,包括白血病和淋巴瘤,相应管线已拿到国家药监局的两个临床批件;二是自身免疫性疾病,包括SLE、坏死性肌炎,相应管线已进入临床前研究阶段。
多位受访者指出,从已有研究来看,CAR-T疗法虽然总体疗效显著,但与普通药物一样,也存在个体差异。任何上市药物的药效都不是100%,这也凸显了临床试验的必要性——需要在尽可能大的人群中证实其疗效。
CAR-T疗法的适用人群,是经过传统治疗后效果不佳或是有效但多次复发的患者。其还不能作为一线治疗方案。传统药物至少已有几十年的临床经验,标准治疗方案无效后,医生再考虑逐步升级疗法。CAR-T疗法经过长期实践形成标准化治疗方案后,才可以讨论作为一线治疗方案的可能性。
适应证方面,CAR-T疗法的优势停留在血液肿瘤领域,即使在自身免疫性疾病领域有所突破,向实体瘤如胃癌、胰腺癌的拓展仍困难重重。已有CAR-T疗法对绝大多数实体瘤的疗效非常有限,原因不明。T细胞要起效,就要在遇到靶细胞后活化分裂,产生更多T细胞,才能把“敌人”完全“剿灭”。有一种可能是,实体瘤的局部环境不利于CAR-T细胞的扩增。
已有越来越多研究专注于改造T细胞的新方法。这涉及更多复杂的免疫学原理,但攻克有望。刘明耀团队也在探索基因编辑与实体瘤CAR-T的结合点,在他看来,未来五年就能看到实体瘤方面的突破。
在保证疗效的基础上,CAR-T疗法的安全性决定了其能否获批。国内外研究报道最多的不良反应是细胞因子释放综合征,也被称为“细胞因子风暴”。即使体内CAR-T疗法也无法完全避免风暴。CAR-T细胞接触到了靶细胞之后,相当于被激活,会伴生细胞因子。这些因子会引发体内炎症反应,表现为发烧、高热。如果炎症因子长时间维持高水平,或引发多器官功能障碍,严重时可致命。
细胞因子风暴在血液肿瘤中更常见,其严重程度跟B淋巴细胞的数量有关。SLE虽然也涉及B淋巴细胞,但数量更少,不良反应相对较轻,临床上观察到患者的发热在24小时之内缓解,发生率也较低,但长期安全性仍有待观察。同时,治疗前使用抗过敏、抗炎药物,能很大程度上减轻风暴。
刘明耀团队治疗过的自身免疫性疾病患者已超过20例,虽然没有完全避免,但尚未观察到较严重的细胞因子风暴。他指出,异体CAR-T的不良反应比传统自体CAR-T更少。
价格成了CAR-T疗法的显著短板。目前国内获批上市的体外CAR-T药物定价都在100万元以上,美国经FDA审批的同类药物定价在十几万到二十万美元。高昂的价格使其普及程度受限。今年CAR-T疗法首次跨过了国家医保谈判门槛,如果纳入商保,这一情况将会得到改善。
体内CAR-T药品的成本显著低于自体CAR-T药物,作为递送基因的载体,其规模化生产工艺已经成熟,光是制造成本就能降至原来的几十分之一甚至百分之一。刘明耀也表示,异体CAR-T把个性化治疗方案转变为真正的货架药品,整体成本可以从百万元级别降到十万元以下,实现平价的可能性非常大。
陈竹团队体内CAR-T药物的研究现在处于I期临床阶段。I期临床纳入了5例复发难治性SLE女性患者,首要目标是探索药物的安全性。在安全的基础上再观察有效性,按照SLE治疗指南,疗效观察通常持续三个月,有初步疗效才会申请Ⅱ期。Ⅱ期、Ⅲ期临床需扩大样本,进一步验证药物在更广大人群中的疗效。
从2012年第一个患者到2017年获批,CAR-T药物已算是快速上市的佼佼者。CAR-T针对的很多难治性疾病还没有标准治疗方案,研究样本量仍很小,且由于伦理问题,临床研究很难设置对照组。一项不到一百例病人的研究,就可能推动一个CAR-T药物获批。国际上,针对自身免疫性疾病的CAR-T疗法,速度最快的药企已完成了Ⅱ期临床,开始准备Ⅲ期,有可能三年后能够看到该疗法获批。而国内可能要五年,而且是从传统的体外CAR-T开始破冰。
业内共识是,从药物靶点发现到上市销售,创新药的研发平均耗时10年、耗资10亿美元,成功率却可能只有1%。去年国内获批上市的SLE靶向生物制剂泰它西普,从研发到上市也经历了近12年。
陈竹团队从2023年开始做临床前研究,2024年底制定了临床研究方案,向医院的伦理委员会提交审查报告,三个月后正式启动了临床试验。伦理审查也是必要的监管环节。体内CAR-T疗法是在体内改造T细胞,药物形式上属于化学药物,还没有划归传统的细胞治疗药物。细胞治疗药物原则上要求医院的伦理委员会以及省级卫生健康部门的两级审批和备案。
对于CAR-T疗法来说,T细胞的改造涉及基因编辑。刘明耀表示,基因编辑的异体CAR-T虽然解决了短期免疫排异的问题,但外源的CAR-T细胞在体内生存时间最多3—6个月,最终会因被排异而失效。“做到3—6个月不被排异,我们付出了八年努力,但伦理审查时还会因为用到了基因编辑技术,而被反复问及伦理风险。”刘明耀说。
监管部门通常面临审核力量不足的问题。如果申报的是领域内第一款药物,监管方面关注的细节会更多,企业申请被驳回的可能性也更大。供应链问题也是一个头疼的问题,许多企业同时有国内和国外的临床管线,在做国内申报时需要把某些原材料换成国产的。目前,监管部门对原材料的管控十分严格。
即使企业联合临床团队,做出了全球最领先、最有望把CAR-T疗法价格打下来的技术,推动产业化落地仍不容易。当前融资环境下,如果缺乏国外的对标产品,资方会“不敢投”。此外,基因与细胞治疗仍在国家发展改革委《市场准入负面清单》中,也就是说,除了试点地区之外,这类企业无法接受外资。
即便如此,近年来,细胞治疗仍迎来了前所未有的发展态势,仅今年全国就有近10家医院启用细胞治疗中心或门诊。今年4月,北京地坛医院肿瘤生物治疗门诊开诊,开展包括免疫治疗、靶向治疗在内的相关临床试验筛选。10月,青海大学附属医院细胞治疗中心成立,填补了该省细胞治疗领域的空白。目前,全国已有超100家医院在国家卫生健康委备案,正式挂牌细胞治疗临床研究科室,提供多种疾病的诊疗服务。
相关新闻
记者调查临床试验抗癌药流入市场 信任危机浮现
重庆宫颈癌患者李忠美抗癌12年后,于2023年再次复发。经医生推荐,她开始使用一种名为卡度尼利单抗的注射药物。然而,用药后她出现了重症肺炎的不良反应
2025-06-02 13:18:34记者调查临床试验抗癌药流入市场重庆通报患者使用临床研究抗癌药 调查结果公布
7月13日,重庆卫生健康和药品监管联合调查组发布了关于患者使用临床研究抗癌药情况的通报。近期,重庆市两名患者使用临床研究抗癌药的情况引起了社会关注
2025-07-14 08:07:34重庆通报患者使用临床研究抗癌药重庆通报2名患者使用抗癌药 调查结果公布
2025-07-14 21:03:31重庆通报2名患者使用抗癌药“中医”自制抗癌药案维持原判 非法制售药品被判刑
2025-05-14 10:22:11中医自制抗癌药案维持原判青岛“中医”自制抗癌药案维持原判 非法制售药品被判刑
2025-05-14 02:46:18青岛中医自制抗癌药案维持原判患者服临床试验抗癌药致重症肺炎 临床研究用药疑云
在重庆39度的高温天气里,刘呈富推着轮椅艰难地爬坡过坎,汗流浃背,呼吸短促。坐在轮椅中的李忠美怀里抱着30多斤重的制氧机,拖着枕头状氧气袋,同样疲惫不堪。李忠美是一位45岁的宫颈癌患者,抗癌已有12年
2025-06-02 14:05:24患者服临床试验抗癌药致重症肺炎