元素周期表是否应重新设计?英媒:或将成为紧迫工作
原标题:元素周期表是否应重新设计?英媒:或将成为紧迫工作
参考消息网3月2日报道 英媒称,有人怀疑现在的元素周期表是否是最佳排列方式。
据英国《新科学家》周刊网站2月26日报道,目前,化学元素是根据原子核中的质子数来排列。而且,元素性质主要是由核外电子的排布所决定的。
最轻的元素只有一个电子层,较重的元素拥有更多电子层。真正决定每种元素性质的是最外层电子数。
元素周期表的排列与外层电子数相关,即具有相同属性的元素被安排在同一族。例如,第一族元素的最外层电子数为1,第二族元素的最外层电子数为2。但它们并不是总能如此完美地匹配。
1.氢应该在哪里?
氢的最外层电子数为1,因此人们可以认为它确实应该排在这个位置,即在第一族内,排在同样只有一个外层电子的锂和钠之后。然而,氢是气体,不是金属,因此它的属性并不匹配。
氢的最外层只有一个电子,它只需得到一个电子即可达到稳定状态,因此,它是一种活泼性很强的元素,从这个意义上说,它与第17族元素更接近,也就是像氯一样的卤族元素。这些元素都只需要获得一个电子即可达到稳定状态。就其性质而言,氢更接近氯而不是锂。
2.为什么汞和金如此怪异?
汞在室温下呈液态。从这个意义上说,它与第12族的其他成员完全不同,它们都是固体金属。
在元素周期表中,越往后的元素,原子核中质子所带正电荷数就越多。这会对核外电子产生更大的吸力,意味着它们必须以越来越快的速度运行。根据爱因斯坦的相对论,这会导致它们的实际质量远远大于电子的正常质量,从而增加内向拉力。汞的电子运行速度高达光速的58%,如此紧密的运行使它们无法与别的原子发生联系,从而无法成为固体。同样的道理也解释了为什么金是金色,它是金属中一种独特的颜色:相对论效应改变了电子吸收光的方式。
推荐阅读

美国夏威夷两座火山持续喷发 当地派出国民警卫队
海外网2022-12-07 10:57:27
美国批准向波兰出售总价值达37.5亿美元的武器装备
央视新闻客户端2022-12-07 10:49:40
西班牙点球大战遭淘汰 葡萄牙大胜瑞士晋级
新华网2022-12-07 10:05:29
布林肯发涉中国防疫言论 中方回应 这几年中国疫情防控方针政策是正确、科学、有效的
环球网2022-12-07 09:36:02
辞职后连夜逃亡的贪官出镜痛哭:东窗事发,一逃了之
2022-12-07 10:17:09
卡塔尔世界杯8强全部出炉 黑马只有一匹:摩洛哥
2022-12-07 11:15:51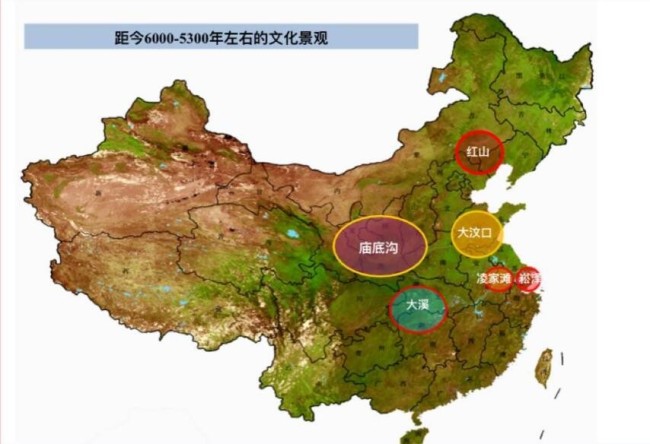
美杂志:中国发现5000年前房屋遗址 人工壕沟等设施展现军事实力
环球网2022-12-07 11:03:30
新冠康复女孩:终于敢承认自己阳过 不好意思曾很压抑自己
2022-12-07 11:02:35
韩国财阀与前总统女儿离婚 并承认自己有婚外子女
海外网2022-12-07 09:41:49
俄媒:泽连斯基正拍卖乌克兰,美国只能借机收割欧洲资本
腾讯网2022-12-07 09:07:33
台积电赴美设厂引多重疑虑 岛内普遍担心台湾将被掏空
环球时报2022-12-07 10:30:14
2023年元旦放假安排来了!元旦放假安排:3天假不调休
2022-12-07 11:07:11
男子买饼需求全被老板说服?网友:没见过这样的pua!
2022-12-07 10:17:45
金毛眼球被抠流落街头被救后离世 多狠毒的心下得去手呢
2022-12-07 10:13:10
胡锡进:我不相信这个国家里会有绝对反对放开封控的人
胡锡进2022-12-07 09:44:10
朝鲜连续实弹射击反制韩美军演 韩军多次向朝鲜发出警告
环球网2022-12-07 09:33:53
大雪节气谁是真正下雪王 乌鲁木齐出人意料夺冠军
2022-12-07 10:27:16
曝李四川接受邀请将出任台北副市长 在蒋万安“三顾茅庐”之后已决定接受蒋邀请
中国台湾网2022-12-07 09:29:51
乌媒:泽连斯基发视频,透露自己在顿巴斯地区 ,庆祝乌克兰“建军节”
新京报2022-12-07 09:11:19
俄总统新闻秘书:普京经常亲自驾车 他常开一辆小电动汽车
中新网2022-12-07 10:40:51
外交部回应朔尔茨文章涉华表态 孤立中国、限制对华合作不符合任何一方利益
新京报2022-12-07 10:57:57
景区回应多人推山顶“风动石”:景区特色 允许推
新京报2022-12-07 10:10:15
坐满士兵的俄军BMP-2步兵战车触雷爆炸画面曝光:大量步兵撤退
环球网2022-12-07 11:09:44
康复患者:我终于敢承认自己阳过
2022-12-07 10:35:40
男孩时隔4个月见父母礼貌喊叔叔 引发无数父母感慨
2022-12-07 10:21:11
乌克兰为何要深入俄腹地空袭?俄罗斯本土连续两天遭袭!
上观新闻2022-12-07 10:34:14
恩师希望梅西拿到世界杯后就退役:那是最好的结局
2022-12-07 10:41:41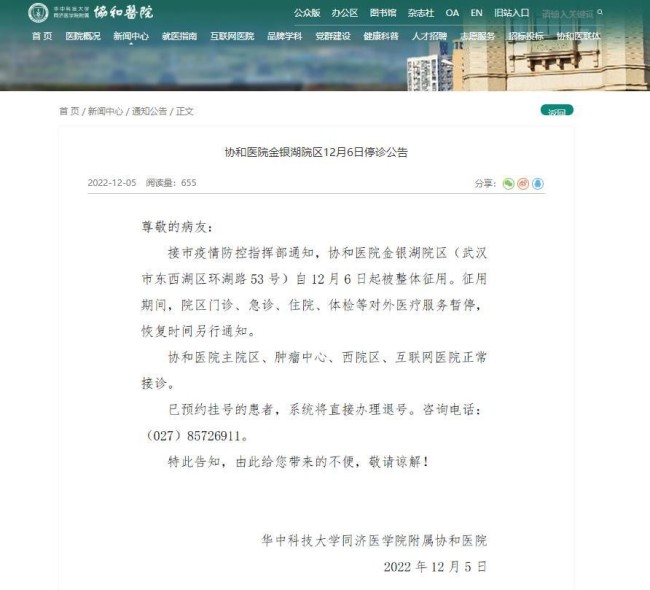
武汉协和医院金银湖院区被整体征用 已在该院区预约挂号的患者,系统将直接办理退号
央广网2022-12-07 09:37:28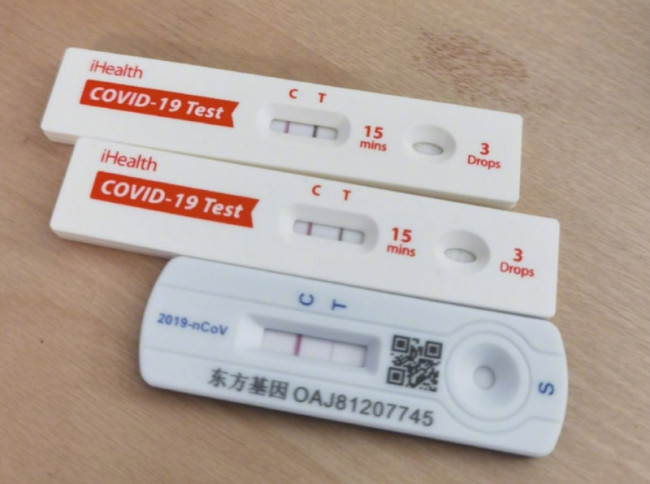
多地零售药店布洛芬和泰诺林售罄,多方回应!
2022-12-07 10:40:14
以色列海上新盾“C-穹顶”问世
海洋防务前沿2022-12-07 09:21:45
落马区委书记贪腐上亿元,被判19年!刚当区长就安排2人伺候
2022-12-07 10:10:05
权威专家:别怕发热 像感冒一样对待!要转变防控重点
2022-12-07 11:11:44
男子醉驾致2死1伤却浑然不知 不知道毁了几个家庭
2022-12-07 10:50:38
俄军装备“上新” 新一批苏-35S战机即将抵达,开足马力生产了
央视网2022-12-07 09:18:01
曝赖清德对接任民进党主席犹豫不决 民进党各派系明争暗斗
海峡导报2022-12-07 09:27:44